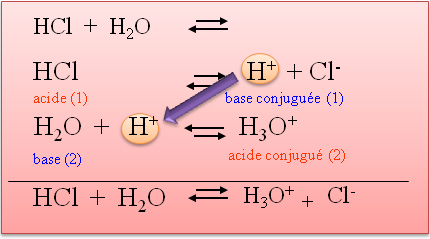
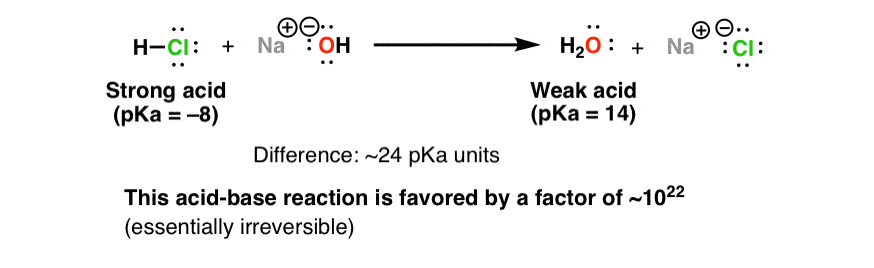
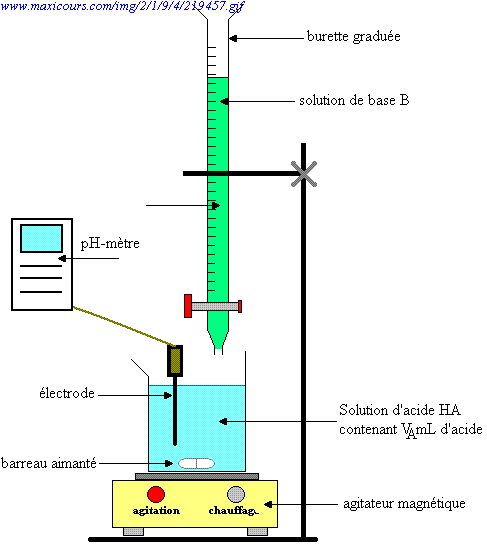
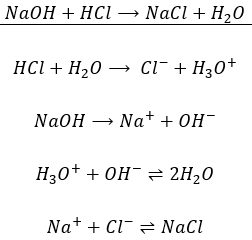Réaction Acide-base. Réaction Chimique Neutralisant Les Propriétés Acides Et Basiques, Produisant Un Sel Et De L'eau. Utilisé Pour Déterminer Le Ph. Bronsted - Théorie De Lowry. Molécules De Hcl, Naoh, H2o Et

Vidéo de question : Calcul du volume d'acide sulfurique nécessaire pour neutraliser complètement une solution d'hydroxyde de sodium de volume et de concentration donnés | Nagwa

Acide-base, Réaction De Neutralisation D'acide Chlorhydrique Et Hydroxyde De Sodium Types De Réactions Chimiques, Partie De 7 Illustration de Vecteur - Illustration du acide, atome: 94216277

SOLVED: Question 4 (1 point) You will determine the concentration of an unknown diprotic acid using your standardized base: The chemical equation for this reaction can be expressed as: Vous determinez la